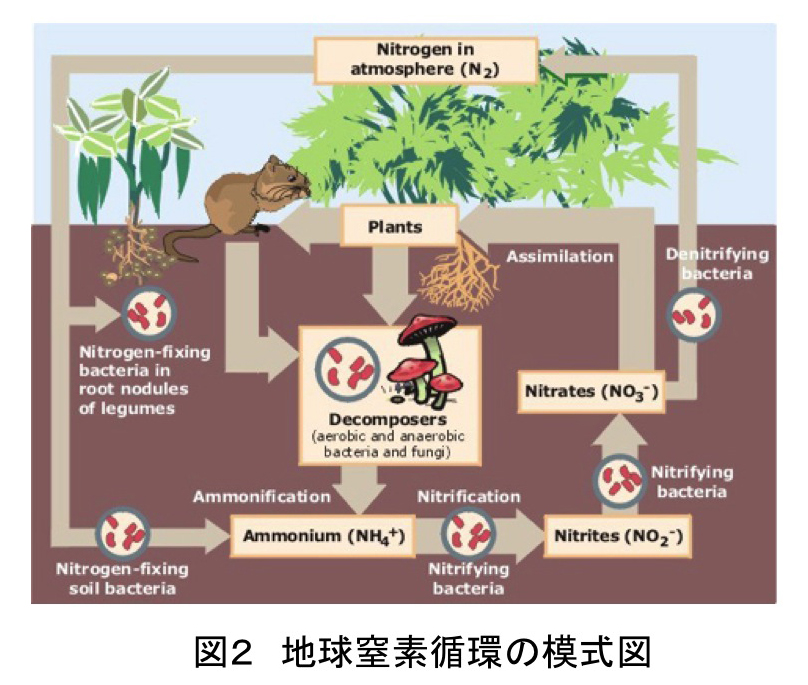
Nitrosomonas europaeaやNitrobacter winogradskyi (以前は、Nitrobacter agilis)は硝化細菌(硝化菌)(図1)と呼ばれ、前者はアンモニアを亜硝酸イオンに、後者は亜硝酸イオンを硝酸イオンに酸化することによりATPを生産し、二酸化炭素を非光合成的に固定する化学合成独立栄養細菌である。これらの細菌は地球窒素循環(図2)や排水処理において重要な役割を担い、地下水の硝酸態窒素による汚染や地球温暖化ガス(N20)の発生にも関わっていることが知られている。従って、硝化細菌(硝化菌)によるアンモニアの硝酸イオンへの変換プロセスを分子レベルで解明することは、上記の環境問題を解決するための手がかりを提供するものと期待される。
生命現象を分子レベルで解明する生化学的研究や構造生物学的研究には、大量の菌体や蛋白質を必要とする。一方、硝化細菌(硝化菌)の生育速度は極めて遅く、さらに収量も低い。例えば、N. winogradskyiを振とう培養すると、定常期でも培養液が僅かに白濁する程度であり、大腸菌の培養液と比べると殆ど“濁り”が無いと判断できるほどである。この問題を解決するには、硝化細菌(硝化菌)を大量に培養する以外に方策はない。幸いにも、私たちは、滅菌可能な500L培養タンクを保有していたので、この培養装置を用いて硝化細菌(硝化菌)を安定に得ることができた。例えば、N. winogradskyiでは、400Lの培養液、130hの培養時間で約30g(湿重量)の菌体を調製することができた。その結果、硝化細菌(硝化菌)の呼吸鎖電子伝達系構成タンパク質を精製し、その酵素的およびタンパク質化学的性質を生化学・分子生物学・構造生物学的手法により明らかにすることができた。以下にこれまでの研究成果を報告する。


N. winogradskyiの好気的呼吸鎖電子伝達系では、呼吸基質として亜硝酸イオン、最終電子受容体として酸素が用いられる。亜硝酸イオンは、亜硝酸—シトクロムc酸化還元酵素により硝酸イオンに酸化される。その際に遊離する電子は、シトクロムcに伝達される。最終的には、シトクロムc酸化酵素がシトクロムcから電子を受け取り、酸素を水に還元することで好気的呼吸鎖電子伝達系が完成する(論文15)。この電子伝達系によりプロトン濃度勾配が形成され、F1FoATP合成酵素によりATPが生産される。
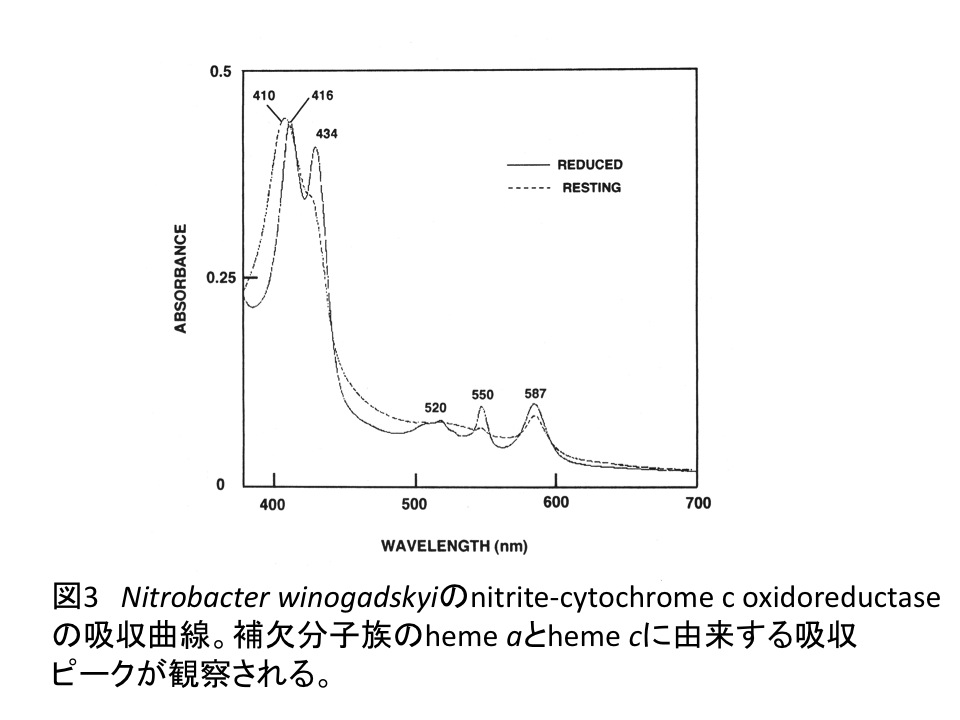
この酵素は膜蛋白質であり、界面活性剤Triton X-100存在下に精製された酵素は3種類のサブユニットI ,II, III (SDS電気泳動では、分子量145K,59K, 30K)で構成されていた。各サブユニットのN末端アミノ酸配列と2006年に決定されたN. winogradskyiのゲノム塩基配列(Appl.Environ.Microbiol.72, 2050-2073, 2006)から、各サブユニットの遺伝子はNwi_774(サブユニットI), Nwi_776(サブユニットII), Nwi_773(サブユニットIII)と推定できる。この酵素は補欠分子族としてヘムa、ヘムc、Fe-Sクラスター、モリブデンコファクターを持ち、その吸収曲線は図3のとおりである。また、この酵素は、pH8付近では、亜硝酸イオンを酸化しシトクロムcを還元する亜硝酸塩—シトクロムc酸化還元酵素活性を示すが、pH6付近では、その酵素活性が低下し、逆反応のフェロシトクロムc—亜硝酸塩酸化還元酵素活性が生じる。すなわち、酸性条件下では、N. winogradskyiは亜硝酸イオンを酸化できないことを強く示唆し、このことがハウス土壌の亜硝酸ガス障害の原因かもしれない。
N. winogradskyiからは2種類のシトクロムcが精製されている。一つは、可溶性のシトクロムc-550(分子量約12500)である。化学的手法により完全決定されたアミノ酸配列はウマのシトクロムcやRhodopseudomonas viridis シトクロムc2のアミノ酸配列と類似していた。また、その遺伝子はNwi_2582と推定でき、本細菌のシトクロムc酸化酵素の電子供与体として機能している。もう一つのシトクロムcは膜結合型であり、分子量は約13600、そのN末端アミノ酸配列から本シトクロムcの遺伝子はNwi_0712と推定できる。また、亜硝酸—シトクロムc酸化還元酵素、シトクロムc酸化酵素および膜結合型シトクロムcをリポソームに再構成したところ、亜硝酸イオンから酸素までの呼吸活性を測定することができた。したがって、亜硝酸から酸素までの電子伝達系は、シトクロムcで分岐している可能性が有る。
N.winogradskyiのシトクロムc酸化酵素は、ヘムaと銅を補欠分子族として持つ、いわゆるヘムー銅シトクロム酸化酵素である。その分光学的性質(酸化型、還元型、CO結合型)は、ミトコンドリアのシトクロムc酸化酵素であるシトクロムaa3と極めて類似しており、840 nmには銅に由来する吸収ピークが観察される。興味深いのは、本酵素が2種類のサブユニット(サブユニットIとサブユニットII)で構成され、それぞれがミトコンドリアDNAにコードされているシトクロムc酸化酵素のサブユニットIとサブユニットIIに相当することである。すなわち、本細菌のシトクロムaa3はミトコンドリアのシトクロムaa3のコア部分と相同であり、ミトコンドリアの起源が細菌である共生説を強く支持する実験結果である。一方、ゲノムからはサブユニットIIIの存在が強く示唆されるが、精製酵素にはサブユニットIIIは存在しない。この原因としては、精製に使用した界面活性剤がTriton X-100であることと関連しているのかもしれない。
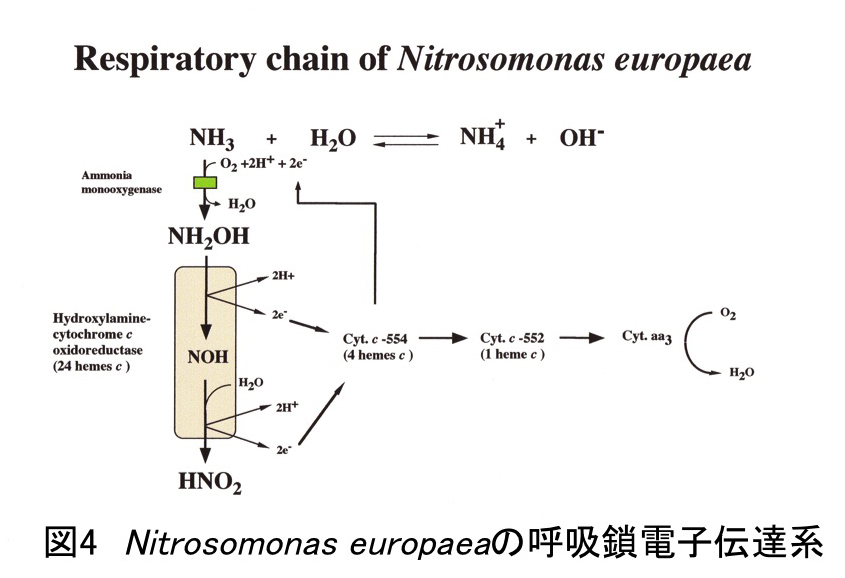
N. europaeaの好気的呼吸鎖電子伝達系では、呼吸基質としてアンモニア、最終電子受容体として酸素が用いられる。アンモニアはアンモニアモノオキシゲナーゼの働きよりヒドロキシルアミンに変換される。その際、電子の供給が必要であるが、その電子供与体は可溶性のシトクロムc-554(あるいはユビキノール)と推定されている。ヒドロキシルアミンはさらにヒドロキシルアミン酸化還元酵素により”NOH”の中間体を経て亜硝酸イオンに酸化されるが、酸素原子は水分子の酸素に由来し、空気中の酸素ではない。この酵素反応で遊離する電子は、シトクロムc-554、さらにシトクロムc-552に伝達される。最終的には、シトクロムc酸化酵素がシトクロムc-552から電子を受け取り、酸素を水に還元することで好気的呼吸鎖電子伝達系が完成する。この電子伝達系によりプロトン濃度勾配が形成され、F1FoATP合成酵素によりATPが生産される(図4)。
N. europaeaのアンモニアモノオキシゲナーゼは極めて不安定であり、未だに、その精製に成功したという報告は無い。しかしながら、Hooper等はアンモニアモノオキシゲナーゼの特異的な阻害剤であるアセチレンが結合する蛋白質を精製し、その蛋白質の遺伝子の塩基配列を決定した (J.Bact.,175, 2436-2444, 1993)。その結果、 Hooper等はN. europaeaのアンモニアモノオキシゲナーゼは2種類のサブユニット(amoA1遺伝子とamoB1遺伝子でコードされている)で構成される膜結合蛋白質であると報告している。一方、N. europaeaのゲノム解析(J. Bacteriol. 185, 2759-2773, 2003)からは第3のサブユニット(amoC1遺伝子でコードされている)の存在が示唆されている。
ヒドロキシルアミン酸化還元酵素(HAO)は、分子量約20万の巨大な蛋白質である。同一サブユニット(546アミノ酸残基)で構成され、3量体構造を形成し、そのアミノ酸配列には、Cys-X1-X2-Cys-His-というヘムc結合モチーフが8カ所ある。また、ヘムcの定量的実験から、各サブユニットは8分子のヘムcを持ち、さらに、8分子のヘムcの内、1つのヘムcは460nmに吸収ピークを示すことからP460と呼ばれている。一方、ヒドロキシルアミンは1度に4電子酸化されて亜硝酸イオンに変換されるのではなく、”NOH”という中間体を経て、2段階の2電子酸化反応により亜硝酸イオンに酸化されることが示唆されている。
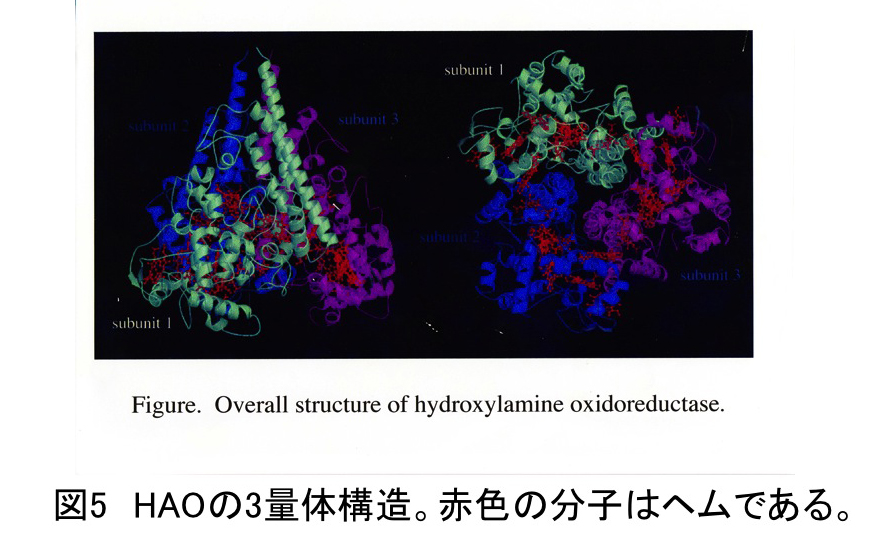
このように、HAOは大変興味ある超分子複合体である。そこで、私たちは、1987年頃からこの酵素の立体構造の解明に取組み、1997年にX線結晶構造解析により2.8Åの分解能で立体構造を決定することに成功した(論文19, 24)。
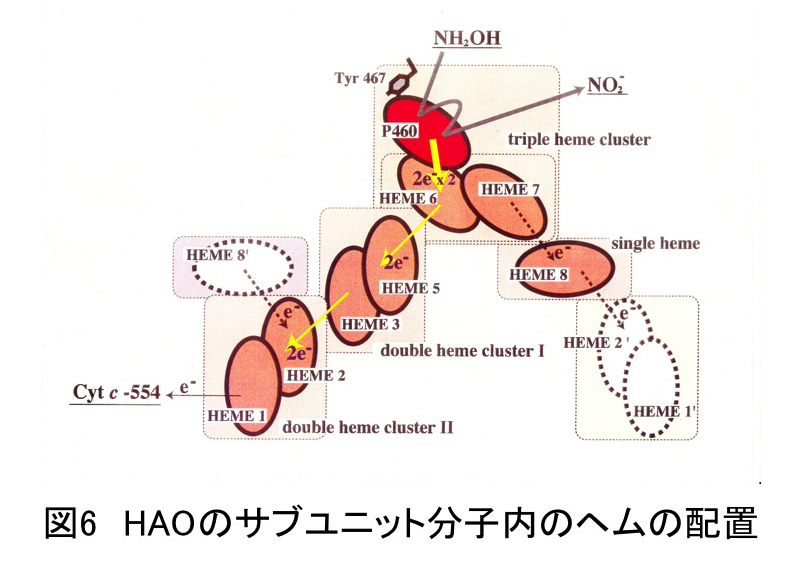
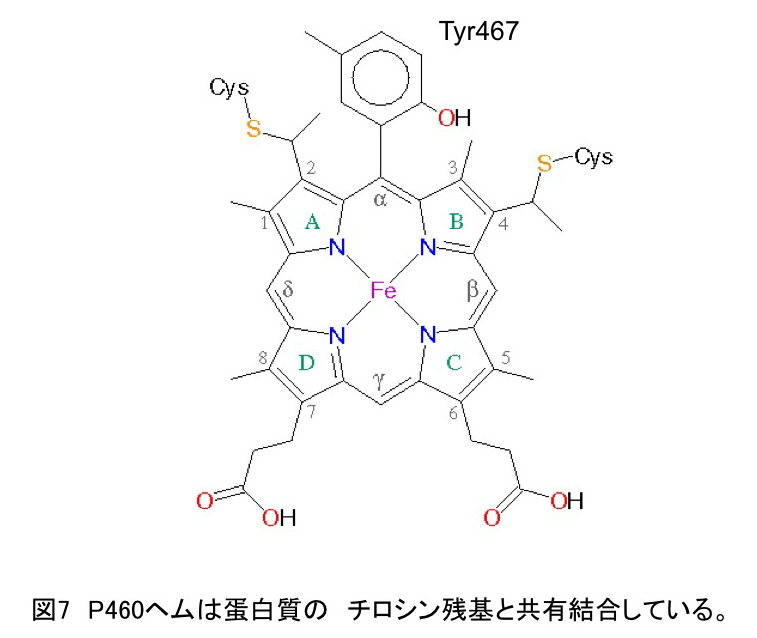
HAOは予想とおり3量体構造を持っていた(図5)。そのサブユニット内には、3分子のヘムcが重なり合ったトリプルヘムクラスターが1つ、2分子のヘムcが重なり合ったダブルヘムクラスターが2つ、そして、シングルヘムcの合計4種類のヘムクラスターが見いだされた(図6)。中でも、トリプルヘムクラスターは全く新しいヘム配置であり、3つのヘムcの内、P460は5配位構造をもち、第6配位座がヒドロキシルアミンの結合部位であることが示唆された。さらに、驚くべきことは、このP460のヘムcのメソ位の炭素にチロシン(Tyr467)残基のベンゼン環炭素が共有結合していたことである(図7)。しかも、このチロシン残基は隣接するサブユニットのチロシン残基であった。すなわち、3量体はヘムcとチロシン残基の共有結合によりつながっていた(このためSDS電気泳動でもモノマー化しなかったのである)。また、ヘムcが重なり合ったトリプルヘムクラスターとダブルヘムクラスターの存在は、2段階2電子反応を可能とする構造的基盤を明確に示す。(詳細は、論文25を参照してください。)
蛋白質の機能を分子レベルで考察することは極めて重要であるが、その際に本質的に必要な情報は立体構造である。私たちは、およそ10年という歳月をかけて、HAOの立体構造を解明した。この研究の遂行に必要な菌体や蛋白質を得るために使用した培養液の容量は約15,000 Lという膨大な量である。幸いにも、私たちの立体構造がNature Structural Biology(論文24)の表紙(図8)を飾ったことは、これまでの努力に報いるものと感謝している。

N. europaeaからは、2種類の可溶性シトクロムc(シトクロムc-554とシトクロムc-552)が精製されている。シトクロムc-554(分子量約25000)は4分子のヘムcを持ち、HAOの電子受容体である。また、シトクロムc-554はHAOのヘムクラスターと類似したダブルヘムクラスターを持っている(Nat.Struc.Biool., 5, 1005-1012, 1998)。このことは、HAOから2電子が同時にシトクロムc-554に伝達されることを強く示唆する。一方、シトクロムc-552は、分子量約9000で1分子のヘムcを持つ蛋白質である。そのアミノ酸配列と立体構造(Biophys.J., 75, 1964-1972, 1998)はPseudomonas属のシトクロムc-551と類似し、本細菌のシトクロムc酸化酵素の電子供与体である。
N. europaeaのシトクロムc酸化酵素は、Erickson等により、その還元型の吸収極大が595nmにあることからシトクロムa1と呼ばれていた。しかしながら、私たちは、N. europaeaのシトクロムc酸化酵素を界面活性剤Triton X-100存在下に精製し、その分光学的性質を検討したところ、還元型の吸収極大は597nmにあったが、COスペクトルやCNスペクトルは、いわゆるaa3型のシトクロムc酸化酵素と同じであることを明らかにした。また、本酵素はヘムaと銅原子を持ち、2種類のサブユニットで構成されていた。さらに、N. europaeaのシトクロムc-552だけでなく酵母やウマなどの真核生物のフェロシトクロムcをもすばやく酸化した。このような特徴は、N. europaeaのシトクロムc酸化酵素がN. vinogradskyiのシトクロムc酸化酵素と同じシトクロムaa3であることを強く示唆する。
N. europaeaやN. winogradskyiは化学合成独立栄養細菌である。すなわち、光合成生物と同じように炭酸固定することにより有機物を生合成する。唯、光合成生物と異なることは光エネルギーを必要としないことである。
これまでの研究によりN. winogradskyiはカルボキシソームを持ち、カルビン回路で炭酸固定を行っていることが明らかとなっている。ゲノム解析から、カルビン回路の2種類の酵素遺伝子が欠損しているが他の遺伝子はすべて存在することが明らかとなっている。その欠損している酵素は、sedoheptulose 1,7-bisphosphatase(EC3.1.3.37)とglyceraldehyde-3-phosphate dehydrogenase(EC1.2.1.13)である。それぞれの代用酵素が存在するが、興味あるのは、EC1.2.1.13の代用酵素がNADH-dependent glyceraldehyde-3-phosphate dehydrogenase(EC1.2.1.12)であり、NADHを利用することである。すなわち、光合成生物とことなりNADPHは必要ないということである。それでは、カルビンベンソン回路に必要なATPとNADHは細胞内でどのような機構で生成しているのだろうか? ATPについては、すでに記述したとおり呼吸鎖電子伝達系とF1FoATPaseにより生成されていることは明らかである。それではNADHは?1963年Aleem等は、N. winogradskyiの無細胞抽出液を用いてATPの添加によりNAD+の嫌気的還元が起こると報告したが(Nature, 200, 759-761, 1963)、私たちの度重なる実験にもかかわらず同じ実験結果は得られなかった。また、1990年には、Bock等がN. winogradskyiにおける亜硝酸イオンによるNAD+の還元はDCCD(F1FoATPaseの阻害剤)により阻害されないと報告し(FEMS Microbiol.Lett., 66, 157-162, 1990)、NAD+還元にATPは必要ないことを示唆した。 一方、N. europaeaのNAD(P)還元系については、そのゲノム解析からNADH-ubiquione oxidoredutaseがプロトン駆動力をもちいて電子を逆流させることでNADHを生成し、さらに、NADPHはプロトン濃度勾配に依存したNAD+/NADP+ transhydrogenaseの働きによりNADHから生成されるという仮説が提案されている。ただ、N. europaeaでもN.winogradskyiと同様にカルビン回路の2つの酵素sedoheptulose 1,7-bisphoshatase(EC3.1.3.37)とglyceraldehyde-3-phosphate dehydrogenase(EC1.2.1.13) の遺伝子が欠損しているが、同じ機能を果たす酵素が存在することから、N.winogradskyiと同じようにNADPHは必要ないのかもしれない。しかしながら、現在に至るまでN.winogradskyiとN. europaeaにおけるNAD+還元系を生化学的に再構成したという報告はない。
1) T.Yamanaka, K.Kamita and Y.Fukumori(1981). Molecular and enzymatic properties of "cytochrome aa3"-type terminal oxidase derived from Nitrobacter agilis. J.Biochem. 89, 265-273.
2) Y.Fukumori and T.Yamanaka(1982). Effect of cardiolipin on the enzymatic activity of Nitrobacter agilis cytochrome c oxidase. Biochim.Biophys.Acta 681, 305-310.
3) Tanaka, Y.Fukumori and T.Yamanaka(1982). The complete amino acid sequence of Nitrobacter agilis cytochrome c-550. Biochim.Biophys. Acta 681, 14-20.
4) T.Yamanaka, Y.Tanaka and Y.Fukumori(1982). Nitrobacter agilis cytochrome c-550;Isolation, physicochemical and enzymatic properties, and primary structure. Plant Cell Physiol. 23, 441-449.
5) Y.Tanaka, Y.Fukumori and T.Yamanaka(1983). Purification of cytochrome a1c1 from Nitrobacter agilis and characterization of nitrite oxidation system of the bacterium. Arch.Microbiol. 135, 265-271.
6) N.Sone, Y.Yanagita, K.Hon-nami, Y.Fukumori, and T.Yamanaka(1983). Proton-pump activity of Nitrobacter agilis and Thermus thermophilus cytochrome c oxidases. FEBS Letters 155, 150-154.
7) M.Sato,N.Tanaka, K.Kakiuchi, Y.Fukumori, T.Yamanaka and M.Kakuno(1983). Small-angle X-ray scattering study on cytochrome aa3-type terminal oxidase derived from Nitrobacter agilis. Biochem.Int. 7, 345-352.
8) Y.Fukumori and T.Yamanaka(1984). Two Km values for cytochrome c of aa3-type two-subunit cytochrome c oxidase from Nitrobacter agilis. FEBS Letters 170, 301-304.
9) Y.Fukumori and T.Yamanaka(1985). Inhibition of an aa3-type two-subunit cytochrome c oxidase from Nitrobacter agilis by N,N-dicyclhexylcarbodiimide. Plant Cell Physiol. 26, 961-965.
10) T.Yamazaki, Y.Fukumori and T.Yamanaka(1985). Cytochrome a1 of Nitrosomonas europaea resembles aa3-type cytochrome c oxidase in many respects. Biochem. Biophys.Acta 810, 174-183.
11) T.Yamazaki, Y.Fukumori and T.Yamanaka(1986). Cytochrome c'-type cytochrome c peroxidase derived from Nitrosomonas europaea. Biochim.Biophys.Acta 871, 36-44.
12) M.Fukuoka, Y.Fukumori and T.Yamanaka(1987). Nitrobacter winogradskyi cytochrome a1 is an iron-sulfur molybdoenzyme having hemes a and c. J. Biochem. 102, 525-530.
13) T.Kurokawa, Y.Fukumori and T.Yamanaka(1987). Purification of a flavoprotein having NADPH-cytochrome c reductase and trans- hydrogenase activities from Nitrobacter winogradskyi and its molecular and enzymatic properties. Arch.Microbiol. 148, 95-99.
14) T.Yamazaki, Y.Fukumori and T.Yamanaka(1988). Catalytic properties of cytochrome c oxidase purified from Nitrosomonas europaea. J.Biochem. 103, 499-503.
15) T.Yamanaka and Y.Fukumori(1988). The nitrite oxidizing system of Nitrobacter winogradskyi. FEMS Microbiol.Rev. 54, 259-270.
16) M.Numata, T.Yamazaki, Y.Fukumori and T.Yamanaka(1989). Some properties of Nitrosomonas europaea cytochrome c oxidase(aa3-type) which lacks CuA. J.Biochem. 105, 245-248.
17) T.Kurokawa, Y.Fukumori and T.Yamanaka(1989). Nitrobacter winogradskyi cytochorme b-559:a nonheme iron-containing cytochrome related tobacterioferritin. Biochim.Biophys.Acta 976, 135-139.
18) Numata M, Saito T, Yamazaki T, Fukumori Y, Yamanaka T. (1990) Cytochrome P-460 of Nitrosomonas europaea: further purification and further characterization. J Biochem., 108, 1016-1021.
19) T.Mikami,N.Tanaka,T.Sato,H.Moriyama,M.Numata,T.Fujiwara,Y.Fukumori, T.Yamanaka,M.Sato, K.Kakiuchi,Y.Katsube and S.Kishimoto(1991). Crystallization and preliminary X-ray studies of hydroxylamine oxidoreductase from Nitrosomonas europaea. J.Biochem. 110, 681-682.
20) Y.Orii, T.Sakamoto.Y.Fukumori and T.Yamanaka(1992). Acceleration of the oxygen reaction in CuA-deficient Nitrosomonas europaea cytochrome c oxidase as revealed by the flow-flash measuremment. Biochim.Biophys.Res.Comm. 182, 1264-1269.
21) T. Nomoto, Y. Fukumori and T. Yamanaka(1993). Membrane-bound cytochrome c is a physiological electron donor for cytochrome aa3 in Nitrobacter winogradskyi. J.Bacteriol. 175, 4400-4404.
22) C.Nagata, N.Igarashi, H.Moriyama, T.Fujiwara, Y.Fukumori and N.Tanaka(1995). Crystallization and preliminary X-ray analysis of cytochrome c-554 from Nitrosomonas europaea. J.Biochem. 117, 931-932.
23) Fujiwara,T., Yamanaka,T. and Fukumori,Y.(1995) The amino acid sequence of Nitrosomonas europaea cytochrome c-552 Curr. Microbiol. 31, 1-4.
24) N.Igarashi, H.Moriyama, T.Fujiwara, Y.Fukumori and N.Tanaka(1997). The 2.8 angstrom structure of hydroxylamine oxidoreductase from a nitrifying chemoautotrophic bacterium, Nitrosomonas europaea. Nat. Struct. Biol., 4, 276-284.
25) 五十嵐教之、藤原健智、福森義宏(1998) ヒドロキシルアミン酸化還元酵素の構造と機能 生化学、70、441—446.